新闻资讯
知识普及
新闻资讯
知识普及
基础知识类
再生医学
再生医学是一门研究如何促进创伤与组织器官缺损生理性修复以及如何进行器官再生与功能重建的新兴学科,其主要通过研究干细胞分化以及机体的正常组织创伤修复与再生等机制,寻找促进机体自我修复与再生,并最终达到构建新的组织与器官以维持、修复、再生或改善损伤组织和器官功能之目的。
从当今的发展趋势看,再生医学已经是现代临床医学中的一种崭新的治疗模式对医学治疗理论、治疗和康复方针的发展有重大影响,也是近年来包括中国在内的世界各国政府重点发展和研究的高新科技领域之一。再生医学的研究范畴在医学科学领域占有重要地位,再生医学的加入是对医学科学理论的发展具有重要意义,其前沿性与现代医学手段和理念的结合将推动医学学科迅速跨上一个前所未有的高度。从近年来快速发展和再生医学所展现的前景看,它已经成为医学研究领域中的一个新的学科,重视再生医学不仅是学科发展、临床应用的需要,同时也是国际竞争的需要。目前我国已经形成了一支优秀的干细胞研究队伍,通过加大投入,假以时日,完全有能力在干细胞与再生医学研究领域赢得一席之地甚至抢夺制高点。
近几十年来,基础医学快速发展,医学研究已经进入分子水平,使得关于人类疾病和健康的知识呈爆炸式增长,人们有理由要求医疗服务水平也随之大幅度提高。为了适应这种要求,推动医学知识转化为医疗服务,转化医学应运而生。转化医学不以拓展人类对疾病和健康的知识为目的,而是研究如何将已有的知识变成现实的医疗服务。这是医学界对目前医学研究模式后的自我批判,也是对社会需求的回应。因此,在基础医学研究还相对落后的情况下,大力发展转化医学研究是适应我国国情、加快我国医学高技术产业发展、提高医疗水平的正确抉择。可以想象,转化医学研究虽然不会为我们赢得诺贝尔奖,但将能够培育出一批有较高知识含金量的原创医疗产品和服务,最终促进我国医疗水平的跨越式发展。
干细胞和再生医学及其相关技术的研究和应用是医学领域未来重要的发展方向,既有重大理论研究价值,又属于国家重大需求,国家已关注干细胞与再生医学的发展现状及重要意义,并加大支持力度,设立干细胞与再生医学学科,以更加有效地推动我国干细胞与再生医学的健康发展。
什么是基因工程技术?
基因工程技术:就是将重组对象的目的基因插入载体,拼接后转入新的宿主细胞,构建成工程菌(细胞),实现遗传物质的重新组合,并使目的基因在工程菌内进行复制和表达的技术。
分子生物学及基因克隆技术改变药物药物研究的途径主要表现在哪些方面?
- 基因克隆和体外表达技术可用来产生人体靶标,当人体组织的来源受到限制甚至不可能时,这种方法显然尤为重要。人原蛋白靶标代替动物蛋白来进行药物筛选具有重要意义。
- 克隆方法可用得尤为重要。人源蛋白靶标代替较为困难或危险的靶标,如从HIV中分离蛋白酶,病毒颗粒中其含量很少,而以生物化学方法分离则需要大量培养这种致命的病原体。
- 用克隆序列进行交叉杂交时确证相关靶标的一种快速方法,考察受试化合物对相关靶标的选择性有助于将药物的不良反应降至最低。
- 定点诱变可用来验证药物相互作用的假设,为药物化学家指出努力方向。
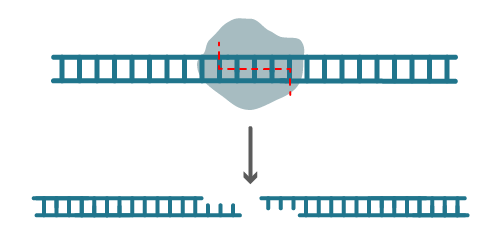
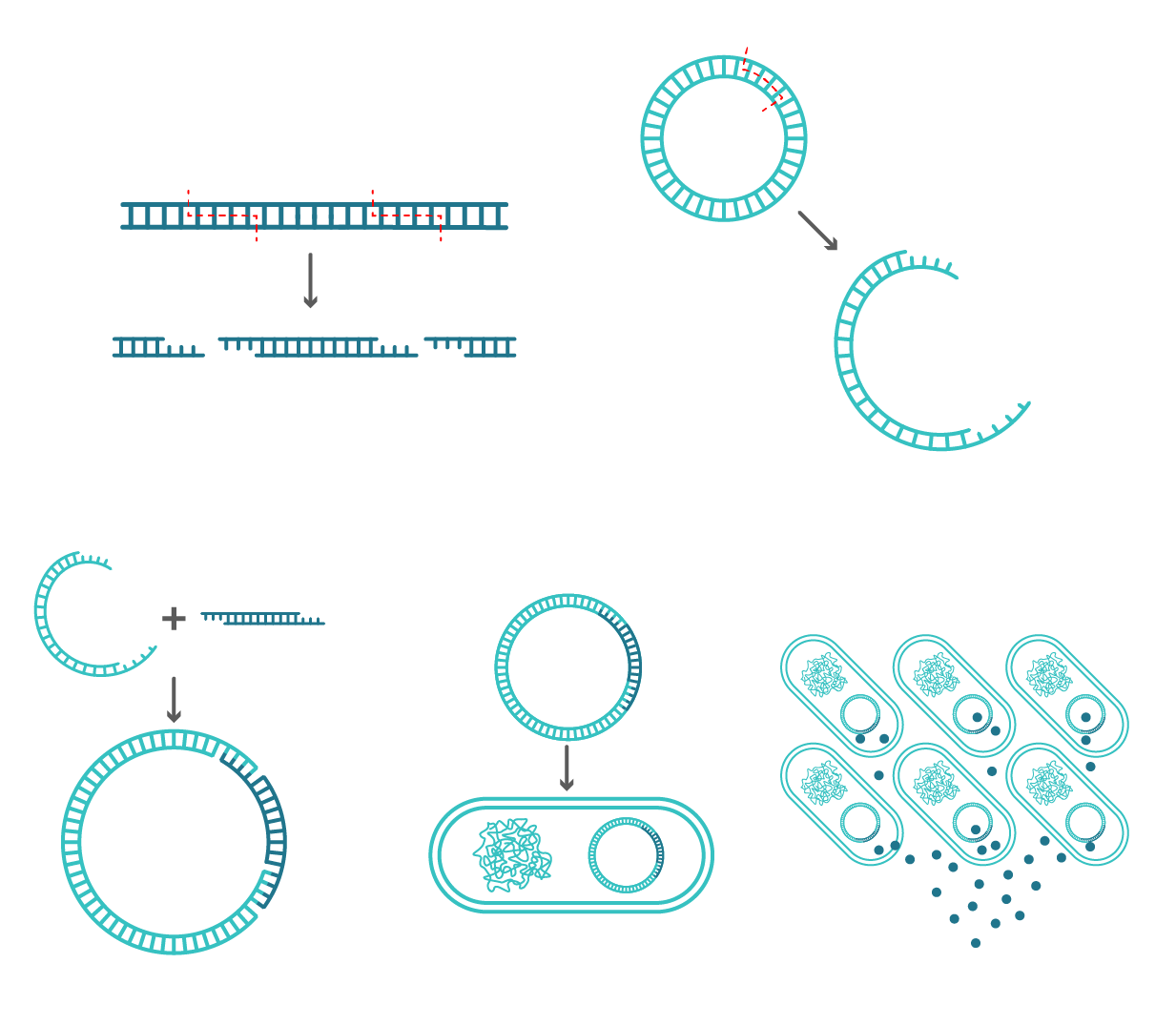
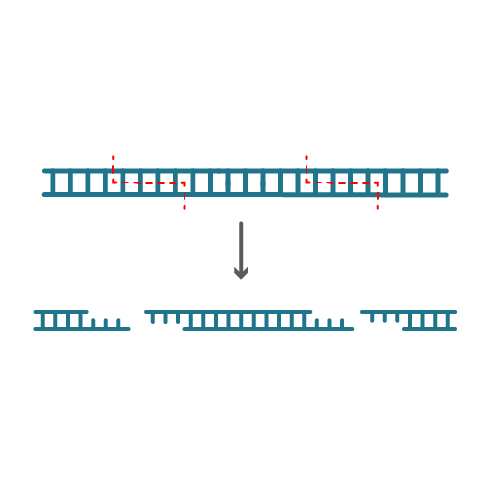
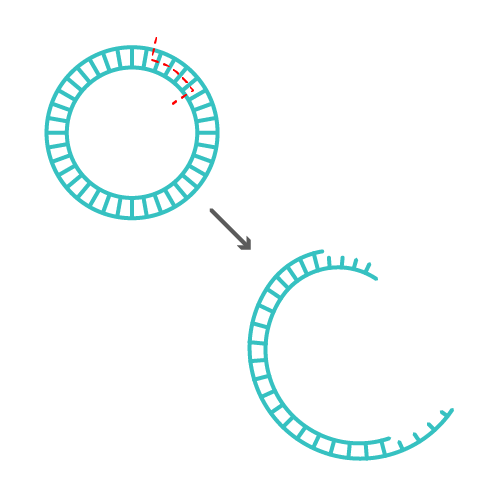
核酸限制性内切酶(restriction endonuclease)
是一类能够识别双链DNA分子上某段特定核苷酸序列,并在该序列中进行切割的核苷内切酶,主要存在于原核微生物中。而在宿主菌中可识别序列的DNA甲基化酶,只对本宿主DNA进行甲基化修饰,从而避免了内切酶对宿主DNA的作用,构成了原核微生物限制-修饰-保护机制的分子基础。
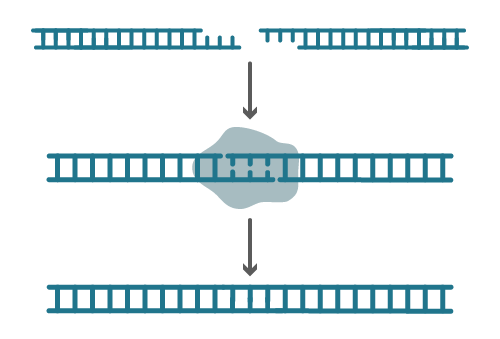
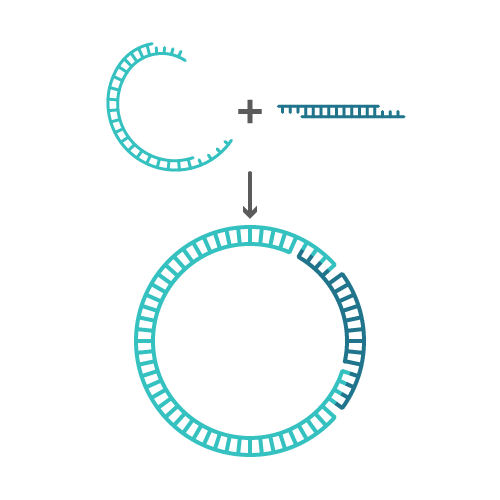
DNA连接酶(DNA ligase)
是催化DNA分子中5’磷酸基与3‘羟基形成磷酸二酯键的酶,DNA连接酶的作用需要ATP和NAD+作为辅助因子,DNA连接酶的底物可以是DNA/RNA杂合体中带缺刻的DNA、黏段DNA或平端DNA,连续效率依次降低。DNA连接酶有两种来源,一种是大肠埃希菌的DNA连接酶,以NAD+作为能源;另一种为T4噬菌体DNA连接酶,以ATP为能源,两种酶作用机制相同。T4 DNA连接酶是从T4噬菌体感染的大肠埃希菌分离得到的,能进行平端DNA片段的链接,因此在基因工程中应用广泛,连接黏端DNA最佳温度为4~15℃。
随着计算机、生物信息、基因合成与基因测序等技术的进展,使计算机辅助设计、全基因乃至基因组人工合成成为可能,使生物工程产业化的技术瓶颈可能突破,使生物产业能够进入工程化与设计化的产业发展,导致了有如“系统科学与自动通讯技术”之间的理论研究与技术转化互动,系统科学与生物技术、系统生物学与合成生物学之间的密切互动,也将导致系统生物技术的基础研究向应用开发的转化(转化科学、转化生物学)距离迅速缩短。
合成生物学
合成生物学(synthetic biology):最初由Hobom B.于1980年提出来表述基因重组技术,随着分子系统生物学的发展,2000年E. Kool在美国化学年会上重新提出来,2003年国际上定义为基于系统生物学的遗传工程和工程方法的人工生物系统研究,从基因片段、DNA分子、基因调控网络与信号传导路径到细胞的人工设计与合成,类似于现代集成型建筑工程,将工程学原理与方法应用于遗传工程与细胞工程等生物技术领域,合成生物学、计算生物学与化学生物学一同构成系统生物技术的方法基础。
合成生物学是指人们将“基因”连接成网络,让细胞来完成设计人员设想的各种任务。例如把网络同简单的细胞相结合,可提高生物传感性,帮助检查人员确定地雷或生物武器的位置。再如向网络加入人体细胞,可以制成用于器官移植的完整器官。让·维斯是麻省理工学院计算机工程师,早在他读研究生时就迷上了生物学,并开始为细胞“编程”,现在已成为合成生物学的领军人物。维斯的导师、计算机工程师和生物学家汤姆·奈特表示,他们希望研制出一组生物组件,可以十分容易地组装成不同的“产品”。研制不同的基因线路———即特别设计的、相互影响的基因。波士顿大学生物医学工程师科林斯已研制出一种“套环开关”,所选择的细胞功能可随意开关。加州大学生物学和物理学教授埃罗维茨等人研究出另外一种线路:当某种特殊蛋白质含量发生变化时,细胞能在发光状态和非发光状态之间转换,起到有机振荡器的作用,打开了利用生物分子进行计算的大门。维斯和加州理工学院化学工程师阿诺尔一起,采用“定向进化”的方法,精细调整研制线路,将基因网络插入细胞内,有选择性地促进细胞生长。维斯目前正在研究另外一群称为“规则系统”的基因,他希望细菌能估计刺激物的距离,并根据距离的改变做出反应。该项研究可用来探测地雷位置:当它们靠近地雷时细菌发绿光;远离地雷时则发红光。维斯另一项大胆的计划是为成年干细胞编程,以促进某些干细胞分裂成骨细胞、肌肉细胞或软骨细胞等,让细胞去修补受损的心脏或生产出合成膝关节。尽管该工作尚处初级阶段,但却是生物学调控领域中重要的进展。
“合成生物学”更早可追踪到波兰科学家Waclaw Szybalski采用“合成生物学”术语,以及目睹分子生物学进展、限制性内切酶发现等可能导致合成生物体的预测。“系统生物学”则可追踪到贝塔朗菲的“有机生物学”及定义“有机”为“整体或系统”概念,以及阐述采用开放系统论、数学模型与计算机方法研究生物学。
药品研发类
新药研发及开发过程介绍
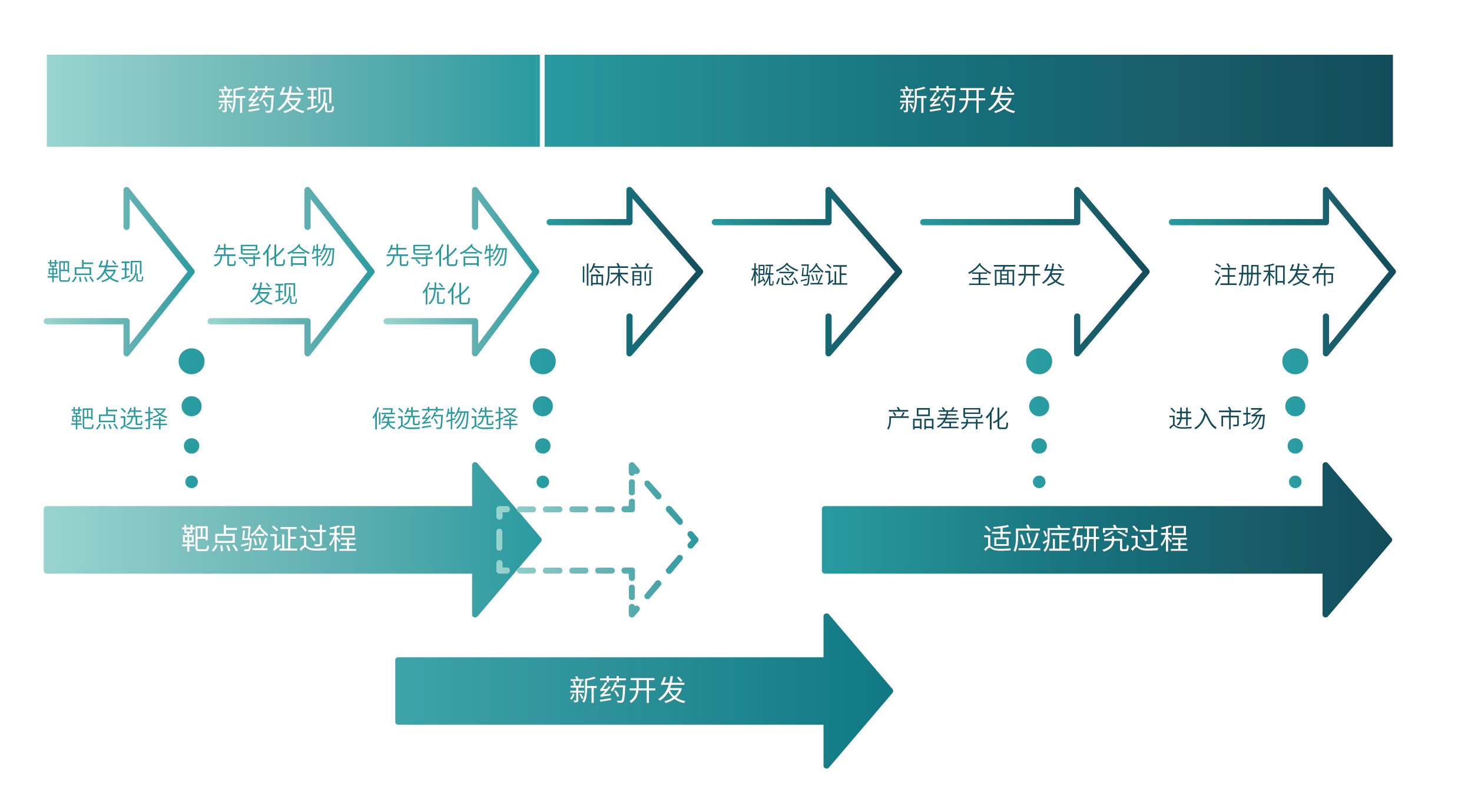
一个药物从发现到开发的全过程一共可以分为两个主要阶段,即药物的发现和药物的开发。第一个阶段是药物的发现,包括从最初的靶点识别到确定单一临床候选药物的全过程。药物发现又包括三个步骤,分别是疾病相关治疗靶点的确认、先导化合物的发现及先导化合物的优化。药物发现过程的每个阶段旨在建立相关靶点与疾病实验模型之间的科学联系。其还包含了靶点的发现、靶标的验证、化合物生物活性筛选、化合物结构改造及优化、才能进入药物的开发阶段。 第二个主要阶段即药物的开发,确定候选化合物后,通过开展各项验证及研究,提供临床前数据,详细介绍动物药效学、毒理学研究结果及化学生产工艺信息,然后通过IND,再提供临床研究的详细方案,才能到达人体临床试验。临床试验还分为I期(考察安全性、耐受性,通常20~100人)、II期(考察安全性、药效性,通常100~300人)、III期(考察药效性、不良反应及副作用,通常近千人)、IV期研究(通常称为上市监测,考察罕见不良反应、联合用药禁忌),总体研究基本目标一致“有效性和安全性”。
新药发现及开发过程概图
药物注册类
化学药品的注册分类
化学药品注册分类介绍:1类、2类(2.1、2.2、2.3、2.4)、3类、4类、5类(5.1、5.2、5.3)
1类:境内外均未上市的创新药。指含有新的结构明确的、具有药理作用的化合物,且具有临床价值的药品。
2类:境内外均未上市的改良型新药。指在已知活性成份的基础上,对其结构、剂型、处方工艺、给药途径、适应症等进行优化,且具有明显临床优势的药品。
2.1含有用拆分或者合成等方法制得的已知活性成份的光学异构体,或者对已知活性成份成酯,或者对已知活性成份成盐(包括含有氢键或配位键的盐),或者改变已知盐类活性成份的酸根、碱基或金属元素,或者形成其他非共价键衍生物(如络合物、螯合物或包合物),且具有明显临床优势的药品。
2.2含有已知活性成份的新剂型(包括新的给药系统)、新处方工艺、新给药途径,且具有明显临床优势的药品。
2.3含有已知活性成份的新复方制剂,且具有明显临床优势。
2.4含有已知活性成份的新适应症的药品。
3类:境内申请人仿制境外上市但境内未上市原研药品的药品。该类药品应与参比制剂的质量和疗效一致。
4类:境内申请人仿制已在境内上市原研药品的药品。该类药品应与参比制剂的质量和疗效一致。
5类:境外上市的药品申请在境内上市。
具体参照注册流程根据《化学药品注册分类及申报资料要求》及《办法》进行合理申报。